AUTORES: GANIX MARIÑELARENA GOYA y DAVID PÉREZ FALAGÁN (2º curso, Grado en Medicina)
Vivimos rodeados de microorganismos. En todo lugar, y en todo momento, estamos en presencia de virus, hongos, bacterias y protozoos. Aunque la mayoría son inofensivos, algunos tienen la capacidad de infectarnos para poder alimentarse y reproducirse. Diseminándose por el aire, el agua, la comida, el contacto directo o el sexual, las enfermedades infecciosas nos han acompañado desde el origen de la especie humana, siendo la principal causa de mortalidad en el mundo. La penicilina, descubierta en 1928 por Alexander Fleming, junto con antibióticos descubiertos con posterioridad (quinolonas, macrólidos, tetraciclinas…), han permitido que las infecciones letales ahora sean problemas menores (1).
Aunque la mayoría de las bacterias son sensibles a los antibióticos, algunas han desarrollado mecanismos para evadirlos y sobrevivir, lo que denominamos resistencia a los antibióticos. Esta resistencia es un proceso que ya ocurre de forma natural, pero décadas de uso y abuso de estos fármacos han acelerado el proceso, dando lugar a cepasde bacterias multirresistentes, inmunes a la mayoría de los antibióticos.
A esta situación se suma el hecho de que la industria farmacéutica y la inversión en investigación se hayan centrado en el desarrollo de medicamentos para patologías crónicas, imposibilitando el descubrimiento de nuevas familias de antibióticos en los últimos 30 años. Esto limita el arsenal antibiótico de los sistemas de salud de todo el mundo y plantea un serio reto para la medicina, la farmacia, la biotecnología y la biomedicina a corto y largo plazo (2).
Datos actuales
En 2016, la Organización Mundial de la Salud (OMS), con el objetivo de visibilizar el problema, incluyó la resistencia bacteriana en la lista de las 10 principales amenazas para la salud a nivel mundial (3). En 2017 emitió la lista de las bacterias para las que se necesitaban urgentemente nuevos antibióticos debido a la frecuencia de cepas multirresistentes. Por orden de prioridad y letalidad serían las siguientes: Staphylococcus aureus, Helicobacter pylori, Pseudomonas aeruginosa o Acinetobacter baumannii (4). El objetivo era concienciar a la comunidad científica y la opinión pública sobre este problema, serio e invisible, que podría ser incluso más letal que el cáncer y costarle a la economía mundial hasta 100 billones de dólares anuales (3).
Así mismo, en España, la Sociedad Española de Medicina de Urgencias y Emergencias señaló en octubre de 2023 que estas superbacterias ya causaban 700.000 muertes al año en todo el mundo (5), 4000 solo en España, 4 veces más que por accidentes de tráfico (6).
Mecanismos de resistencia de las bacterias
En primer lugar, cabe recalcar que las bacterias pueden ser intrínsecamente resistentes a los antibióticos que utilizamos, ya sea por su estructura o características funcionales. Por ejemplo, si un antibiótico va en contra de una molécula específica presente en diversas bacterias, aquellas que no la presenten serán resistentes al antibiótico (7). Además, las bacterias pueden adquirir resistencias mediante tres mecanismos principales (7):
1. Disminución de la concentración de antibiótico dentro de la bacteria. Esto se logra evitando que el antibiótico pase al interior de la célula regulando el número de canales presentes en su membrana (porinas) o expulsándolo mediante moléculas similares a bombas de extracción.
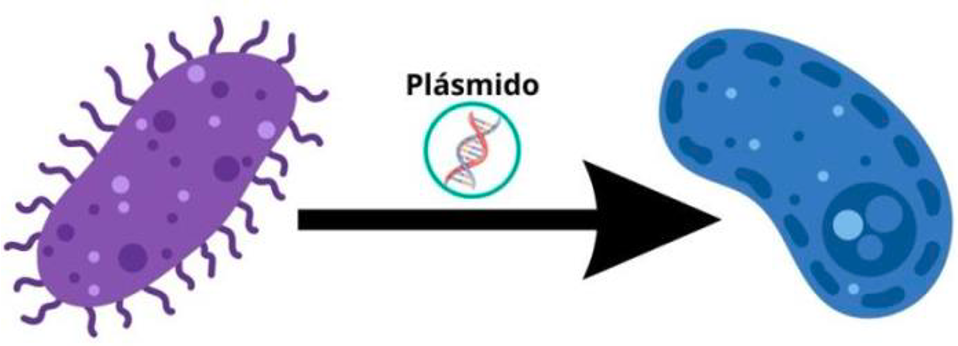
2. Modificación de la diana contra la que actúa el antibiótico para impedir su unión. Si se da alguna mutación que modifica el material genético o una bacteria adquiere un plásmido (material genético intercambiable entre bacterias gracias a un proceso llamado conjugación), el antibiótico puede perder su eficacia debido a que no reconoce su diana frente a la que ha sido diseñado (Figura 1).
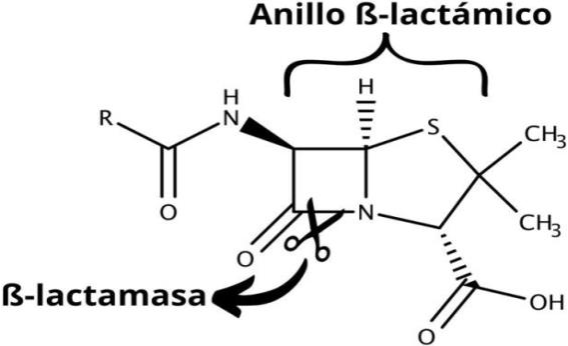
3. Modificación del antibiótico. Existen bacterias capaces de producir diversas moléculas llamadas enzimas, capaces de alterar la estructura de los antibióticos. Un ejemplo de estas enzimas son las ß-lactamasas, que alteran la estructura de los antibióticos ß-lactámicos como la penicilina (Figura 2).
Posibles soluciones a la resistencia a los antibióticos
El desarrollo de nuevos antibióticos no es la respuesta inmediata a esta problemática, con lo que la solución más temprana y temporal al problema es la vigilancia epidemiológica y un mayor comedimiento en la prescripción de estos medicamentos. Por ejemplo, en España el Plan Nacional frente a la Resistencia a Antibióticos (PRAN) se encarga de ello, aportando datos como el consumo de antibióticos por comunidad autónoma por ejemplo. Además, trabaja en todo el territorio nacional para la implantación de los Programas de Optimización de Uso de los Antibióticos (PROA) tanto en el ámbito hospitalario como en el de Atención Primaria. Estos programas trabajan en la optimización de la prescripción de antibióticos para mejorar el pronóstico de los pacientes que los necesitan, minimizar los efectos adversos, controlar la aparición de resistencias y garantizar el uso de tratamientos coste- efectivos (8).
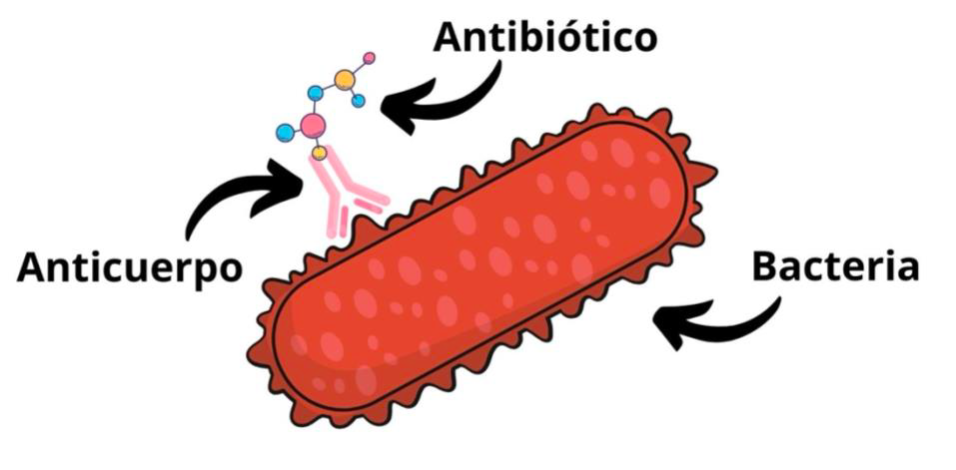
Además de estos planes, se plantean nuevas terapias para poder hacer frente a los microorganismos que nos infectan. La vacunación podría ayudar a disminuir las resistencias generadas por el uso de los antibióticos tradicionales (9). Otra de las terapias se basa en dirigir el fármaco a los componentes que no sean esenciales del microorganismo, pero que jueguen un papel importante en el desarrollo de la enfermedad. Por ejemplo, se podrían utilizar anticuerpos unidos al antibiótico que se dirijan de manera específica a un componente de la bacteria (Figura 3). De esta manera no se generarían tantas cepas resistentes y no eliminaríamos a las bacterias que residen en nuestro organismo (la conocida microbiota, muy importante en el combate de infecciones por bacterias patógenas) (9).
También se ha propuesto el uso de unos virus que se caracterizan por infectar bacterias: los bacteriófagos. Además de eliminar directamente a la bacteria, se pueden utilizar como medio de transporte para insertar un complejo molecular conocido como CRISPR-Cas9 dentro de la bacteria. Este sistema tiene como objetivo modificar los genes de las bacterias para eliminar las resistencias. Sin embargo, tanto la terapia con estos virus como la modificación genética mediante CRISPR están todavía en investigación (9).
Consejos para evitar que la resistencia a los antibióticos empeore
- Toma los antibióticos solo cuando la infección contraída esté causada por bacterias, ya que los antibióticos no tienen efecto sobre infecciones víricas.
- Sigue las pautas de tratamiento que el médico te ha prescrito. Aunque te sientas mejor sin haber finalizado el tratamiento, tomarlo hasta el final es muy importante para erradicar la infección.
- No almacenes los antibióticos y deséchalos al acabar el tratamiento.
- No utilices antibióticos si tu médico no te los ha recetado, y no los pidas prestados a otra persona (10).
Conclusiones y mensaje para recordar
Tras haber analizado el problema que supone la resistencia a los antibióticos, es fundamental que tanto los profesionales de la salud como la población realicemos un uso adecuado y comedido de los antibióticos para que no se creen más resistencias y podamos seguir usando estos medicamentos de manera efectiva. Aunque los planes que se han establecido para la optimización del uso de antibióticos y las nuevas terapias puedan solucionar en parte este problema, resulta indispensable la colaboración de toda la población para evitar más muertes causadas por la resistencia a los antibióticos.
Bibliografía
1. La penicilina, el descubrimiento más afortunado de Alexander Fleming, historia.nationalgeographic.com.es (2019). https://historia.nationalgeographic.com.es/a/alexander-fleming-padre-penicilina_14562.
2. Por qué es tan difícil desarrollar nuevos antibióticos, BBC News Mundo. https://www.bbc.com/mundo/noticias-41776539.
3. Bacterias multirresistentes: por qué es necesaria una acción inmediata. https://www.who.int/es/news-room/commentaries/detail/superbugs-why-we-need-action-now.
4. La OMS publica la lista de las bacterias para las que se necesitan urgentemente nuevos antibióticos. https://www.who.int/es/news/item/27-02-2017-who-publishes-list-of-bacteria-for-which-new-antibiotics-are-urgently-needed.
5. Las bacterias multirresistentes ya causan 700.000 muertes cada año en el mundo, SEMES(2023). https://www.semes.org/las-bacterias-multirresistentes-ya-causan-700-000-muertes-cada-ano-en-el-mundo/.
6. S. Y. Medicina, En España mueren al año 4.000 personas por infecciones debidas a bacterias multirresistentes (2021). https://www.saludymedicina.org/post/en-espana-mueren-al-ano-4-000-personas-por-infecciones-debidas-a-bacterias-multirresistentes.
7. J. M. A. Blair, M. A. Webber, A. J. Baylay, D. O. Ogbolu, L. J. V. Piddock, Molecular mechanisms of antibiotic resistance. Nat. Rev. Microbiol.13, 42–51 (2015).
8. Programas de Optimización de Uso de los Antibióticos (PROA) | PRAN. https://www.resistenciaantibioticos.es/es/lineas-de-accion/control/programas-de-optimizacion-de-uso-de-los-antibioticos-proa.
9. V. Bhandari, A. Suresh, Next-Generation Approaches Needed to Tackle Antimicrobial Resistance for the Development of Novel Therapies Against the Deadly Pathogens. Front. Pharmacol.13(2022).
10. Qué hacer y qué no hacer con los antibióticos | Prescripción y uso de antibióticos | CDC (2022). https://www.cdc.gov/antibiotic-use/sp/do-and-dont.html.